Kemičari s MIT-a uspjeli su rekonstruirati protein koji ima mogućnost izbacivanja toksina iz bakterijskih stanica. Vjeruje se da upravo proteini poput ovoga omogućuju bakterijama poput E. coli da steknu rezistenciju na antibiotike.
Koristeći spektroskopiju nuklearne magnetne rezonancije (NMR), istraživači su promatrali kako se mijenja struktura ovog proteina dok se kroz njega kreće molekula nalik lijeku. Upravo poznavanje takvih promjena omogućuje znanstvenicima daljnji razvoj lijekova koji bi zaobišli ovaj mehanizam izbacivanja. Najrealniji je scenarij da se stvori lijek koji bi bio identičan trenutačnim osim što bi sadržavao dodatne strukture koje bi se natjecale za vezno mjesto s antibioticima te na taj način spriječile njihovo izbacivanje iz stanice.
Transporteri odgovorni za otpornost na lijekove
Izbacivanje lijekova kroz njihove stanične membrane jedna je od mnogih strategija koje bakterije koriste kako bi se obranile od antibiotika. Ovaj tim znanstvenika već neko vrijeme promatra proteine koji su zaduženi za izbacivanje antibiotika iz stanice. Najviše su se usmjerili na protein pod nazivom EmrE. Navedeni protein može prenositi različite toksične molekule, uključujući herbicide i antimikrobne lijekove.
EmrE pripada obitelji proteina pod nazivom „multidrug transporters“ koji su zaduženi za rezistencije na brojne antibiotike. Iako EmrE nije direktno uključen u mehanizam rezistencije, ostali članovi obitelji pronađeni u Mycobacterium tuberculosis i Acinetobacter baumanii jesu.
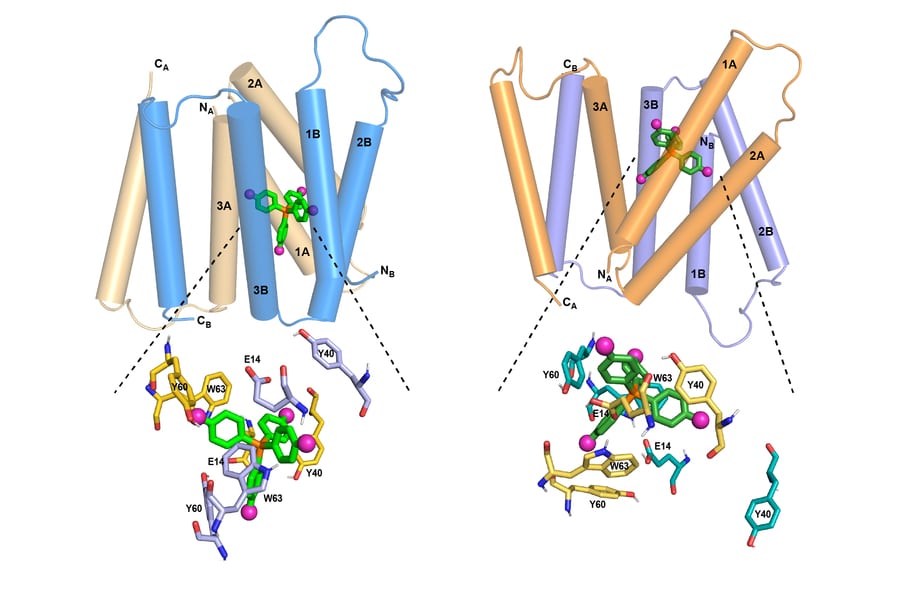
Za razliku od ostalih proteina, EmrE se relativno lako proučava i s obzirom na sličnost u genskim sekvencama, može poslužiti kao idealan modelski sustav za proučavanje.
EmrE prenosi otrovne molekule (otrovne za bakterijsku stanicu) iz unutrašnjosti stanice, koja ima neutralan pH, prema van, gdje je pH kisel. Ova promjena pH vrijednosti membrane utječe na strukturu EmrE.
EmrE protein je izgrađen od četiri spirale i bočnih lanaca. Pri neutralnom pH te spirale su postavljene paralelno jedna s drugom, pri čemu se stvara otvor u koji molekula lijeka može lako ući. Kako pH pada prema vanjskoj membrani, tako se mijenja konformacija spirala te kanal postaje otvoreniji prema vanjskoj strani stanice.
Ovaj rad upotpunjuje priču o strukturi i funkciji transmembranskih proteina koji omogućuju pojavu rezistencije raznim bakterijama. Vjeruje se da će ovo znanje uvelike doprinijeti farmaceutskim firmama pri dizajniranju novih lijekova.